脂肪组织在减重后保留了肥胖的表观遗传记忆——基于**Adipose tissue epigenetic memory of obesity after weight loss**的研究
您的隐私,您的选择
我们使用必要的 Cookies 来确保网站正常运行。我们还会使用可选的 Cookies 用于广告、内容个性化、使用情况分析和社交媒体。
通过接受可选 Cookies,您同意处理您的个人数据,包括传输给第三方。某些第三方位于欧洲经济区之外,数据保护标准各不相同。
请参阅我们的隐私政策,了解更多关于您的个人数据的使用信息。
管理偏好以获取更多信息并更改您的选择。
接受所有 Cookies
感谢访问 nature.com。您使用的浏览器版本对 CSS 的支持有限。为了获得最佳体验,我们建议您使用更新的浏览器(或关闭 Internet Explorer 中的兼容模式)。同时,为了确保持续支持,我们将在没有样式和 JavaScript 的情况下显示该网站。
广告
搜索
按主题、关键字或作者搜索文章
显示来自 所有期刊 本期刊 的结果
搜索
快速链接
* [按主题浏览文章](https://www.nature.com/articles/</subjects>)
* [查找工作](https://www.nature.com/articles/</naturecareers>)
* [作者指南](https://www.nature.com/articles/</authors/index.html>)
* [编辑政策](https://www.nature.com/articles/</authors/editorial_policies/>)
浏览内容
* [研究文章](https://www.nature.com/articles/</nature/research-articles>)
* [新闻](https://www.nature.com/articles/</news>)
* [观点](https://www.nature.com/articles/</opinion>)
* [研究分析](https://www.nature.com/articles/</research-analysis>)
* [职业](https://www.nature.com/articles/</careers>)
* [书籍与文化](https://www.nature.com/articles/</books-culture>)
* [播客](https://www.nature.com/articles/</nature/podcasts>)
* [视频](https://www.nature.com/articles/</nature/videos>)
* [当前期刊](https://www.nature.com/articles/</nature/current-issue>)
* [浏览期刊](https://www.nature.com/articles/</nature/browse-issues>)
* [合集](https://www.nature.com/articles/</nature/collections>)
* [主题](https://www.nature.com/articles/</nature/browse-subjects>)
* [在 Facebook 上关注我们](https://www.nature.com/articles/<https:/www.facebook.com/Nature>)
* [在 Twitter 上关注我们](https://www.nature.com/articles/<https:/twitter.com/nature>)
* [注册提醒](https://www.nature.com/articles/<https:/www.nature.com/my-account/alerts/subscribe-journal?list-id=1>)
* [RSS 源](https://www.nature.com/articles/<https:/www.nature.com/nature.rss>)
关于本期刊
* [期刊员工](https://www.nature.com/articles/</nature/journal-staff>)
* [关于编辑](https://www.nature.com/articles/</nature/editors>)
* [期刊信息](https://www.nature.com/articles/</nature/journal-information>)
* [我们的出版模式](https://www.nature.com/articles/</nature/our-publishing-models>)
* [编辑价值声明](https://www.nature.com/articles/</nature/editorial-values-statement>)
* [期刊指标](https://www.nature.com/articles/</nature/journal-impact>)
* [奖项](https://www.nature.com/articles/</nature/awards>)
* [联系方式](https://www.nature.com/articles/</nature/contact>)
* [编辑政策](https://www.nature.com/articles/</nature/editorial-policies>)
* [Nature 的历史](https://www.nature.com/articles/</nature/history-of-nature>)
* [发送新闻提示](https://www.nature.com/articles/</nature/send-a-news-tip>)
与我们一起出版
* [致作者](https://www.nature.com/articles/</nature/for-authors>)
* [致审稿人](https://www.nature.com/articles/</nature/for-referees>)
* [语言编辑服务](https://www.nature.com/articles/<https:/authorservices.springernature.com/go/sn/?utm_source=For+Authors&utm_medium=Website_Nature&utm_campaign=Platform+Experimentation+2022&utm_id=PE2022>)
* [提交稿件](https://www.nature.com/articles/<https:/mts-nature.nature.com/>)
脂肪组织在减重后保留了肥胖的表观遗传记忆
- 文章
- 开放获取
- 发布时间:2024 年 11 月 18 日
脂肪组织在减重后保留了肥胖的表观遗传记忆
- Laura C. Hinte ORCID: orcid.org/0000-0002-4226-00091,2 na1,
- Daniel Castellano-Castillo1 na1 nAff8,
- Adhideb Ghosh ORCID: orcid.org/0000-0002-5160-45711,3,4,
- Kate Melrose ORCID: orcid.org/0000-0002-0170-08131,2,
- Emanuel Gasser1,
- Falko Noé ORCID: orcid.org/0009-0002-3360-54551,3,4,
- Lucas Massier5 nAff9,
- Hua Dong4 nAff10,
- Wenfei Sun ORCID: orcid.org/0000-0001-5762-60104 nAff11,
- Anne Hoffmann ORCID: orcid.org/0000-0003-3258-33976,
- Christian Wolfrum ORCID: orcid.org/0000-0002-3862-68054,
- Mikael Rydén ORCID: orcid.org/0000-0003-4785-18765,
- Niklas Mejhert ORCID: orcid.org/0000-0003-1785-833X5,
- Matthias Blüher ORCID: orcid.org/0000-0003-0208-20656,7 &
- …
- Ferdinand von Meyenn ORCID: orcid.org/0000-0001-9920-30751
显示作者 Nature volume 636, pages 457–465 (2024)引用这篇文章
- 280k 次访问
- 4043 Altmetric
- 指标详情
摘要
降低体重以改善代谢健康和相关合并症是治疗肥胖症的主要目标1,2. 然而,保持减重是一个相当大的挑战,特别是当身体似乎保留了一种致肥胖的记忆,以抵抗体重变化3,4. 克服长期治疗成功的这一障碍是困难的,因为支撑这种现象的分子机制在很大程度上仍然未知。在这里,通过使用单核 RNA 测序,我们表明人类和小鼠的脂肪组织在明显的减重后都保留了细胞转录变化。 此外,我们发现小鼠脂肪细胞表观基因组中持续存在肥胖诱导的改变,这些改变对其功能和对代谢刺激的反应产生负面影响。 携带这种致肥胖记忆的小鼠表现出加速的反弹体重增加,并且表观遗传记忆可以解释脂肪细胞在对进一步高脂饮食喂养作出反应时,未来转录失调的原因。 总之,我们的研究结果表明,在小鼠脂肪细胞中,可能在其他细胞类型中,存在一种主要基于稳定的表观遗传变化的致肥胖记忆。这些改变似乎启动了细胞在致肥胖环境中的病理反应,导致了节食中经常出现的有问题的“溜溜球”效应。 未来针对这些改变可能改善长期体重管理和健康结果。
其他人正在浏览的类似内容
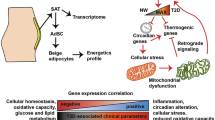
2 型糖尿病进展中的转录动态与人类脂肪组织中的昼夜节律、产热和细胞应激有关
文章 开放获取 2025 年 3 月 8 日
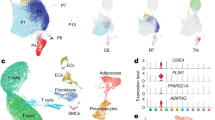
snRNA-seq 揭示了一个调节产热的脂肪细胞亚群
文章 2020 年 10 月 28 日

胰岛素抵抗重新连接代谢基因程序和人白色脂肪细胞中的葡萄糖利用
文章 2021 年 11 月 19 日
主要内容
肥胖及其相关合并症代表着重大的健康风险1. 管理肥胖的主要临床目标是实现明显的减重 (WL),通常通过严格的饮食和生活方式干预、药物治疗或减重手术 (BaS)2. 依赖于行为和饮食改变的策略通常仅导致短期 WL,并且容易受到“溜溜球”效应的影响,在这种效应中,个体随着时间的推移而恢复体重3,5,6. 这种复发模式可能部分归因于即使在显著的 WL 之后仍然存在的(致肥胖)代谢记忆4,7,8,9,10 或代谢改善11,12,13. 事实上,先前代谢状态的持久表型变化,即代谢记忆,已在小鼠脂肪组织 (AT) 或基质血管成分 (SVF) 中得到报告14,15,16, 而在肝脏中这些变化是可逆的15,16,17. 免疫系统18 以及许多器官的内皮细胞中的转录和功能记忆19,20,21,22 在 WL 后的持续改变也已得到报告。
表观遗传机制和修饰对于体外和体内脂肪细胞的发育、分化和身份维持至关重要23,24,25,26,27, 但预计也是肥胖细胞记忆的关键贡献者4,7. 例如,持久的染色质可及性变化与小鼠骨髓细胞中肥胖的病理记忆有关28, 并且冷暴露研究也表明存在(表观遗传)细胞记忆26,29. 迄今为止,大多数人类研究都集中在对整体组织或全血进行 DNA 甲基化分析,以评估推定的细胞记忆[30](https://www.nature.com/articles/<#ref-CR30> "Barres, R. et al. Weight loss after gastric bypass surgery in human obesity remodels promoter methylation. Cell Rep. 3, 1020–10
